अम्ल, क्षारक और लवण
अम्ल और क्षारक में समानताएँ
अम्ल और क्षारक का जलीय विलयन
जब अम्ल को जल में घुलाया जाता है तो यह हाइड्रोजन आयन (H+) देता है। यह नीचे दिये गये समीकरण में दिखाया गया है।
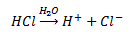
हाइड्रोजन आयन अकेले नहीं रह सकते हैं। इसलिये हाइड्रोजन आयन जल के एक अणु के साथ मिलकर हाइड्रोनियम आयन बनाता है। यह नीचे दिये गये समीकरण में दिखाया गया है।
H + + H2O ⇨ H3O +
जब किसी क्षारक को जल में घुलाया जाता है तो यह हाइड्रॉक्साइड आयन बनाता है। यह नीचे दिये गये समीकरण में दिखाया गया है।
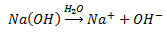
नोट: जो क्षारक जल में घुलनशील होते हैं उन्हें अल्काली या क्षार कहते हैं।
हाइड्रोजन आयन और हाइड्रोनियम आयन के निर्माण के संदर्भ में उदासीनीकरण की परिभाषा निम्न तरीके से की जाती है।
Acid + Base ⇨ Salt + Water
HX + MOH ⇨ MX + HOH
H + (aq) + OH -(aq) ⇨ H2O
जब एक अम्ल या क्षारक को जल में मिलाया जाता है तो हाइड्रोजन आयन या हाइड्रोनियम आयन की सांद्रता घट जाती है। इससे अम्ल या क्षारक का तनुकरण (dilution) होता है।
अम्लीय और क्षारीय विलयन की प्रबलता
अम्लीय और क्षारीय विलयन की प्रबलता को pH स्केल से दिखाया जा सकता है। pH की अधिक सांद्रता का मतलब होता है अधिक अम्लीयता। pH स्केल का रेंज जीरो से 14 तक होता है। हाइड्रोजन आयन की अधिक सांद्रता का मतलब होता है pH का कम मान। एक उदासीन विलयन के pH का मान 7 होता है। अम्लीय विलयन के pH का मान 7 से कम होता है और क्षारीय विलयन के pH का मान 7 से अधिक होता है।
यूनिवर्सल इंडिकेटर: यह कई सूचकों का मिश्रण होता है। यह इंडिकेटर pH के अलग-अलग मानों के लिये अलग-अलग रंग दिखाता है। इसके लिये यूनिवर्सल इंडिकेटर लगे हुए पेपर का इस्तेमाल किया जाता है।
दैनिक जीवन में pH का महत्व
सजीवों में pH की रेंज:मानव शरीर 7.0 से 7.8 तक की pH रेंज में काम करता है। ज्यादातर सजीव इसी रेंज में काम करते हैं। यदि वातावरण का pH अम्लीय या क्षारीय हो जाता है तो यह सजीव के लिये नुकसानदेह साबित होता है। इसलिये अम्लीय वर्षा जलीय पादपों और जंतुओं के लिये हानिकारक होती है।
मिट्टी और pH:मिट्टी का pH पादपों के सही विकास के लिये बहुत महत्वपूर्ण होता है। अम्लीय या क्षारीय मिट्टी में फसल की उपज ठीक नहीं होती है। मिट्टी के pH को सही रेंज में रखने के लिये किसानों को मिट्टी का समुचित उपचार करना पड़ता है। अम्लीय मिट्टी में किसान को चूना डालना पड़ता है। क्षारीय मिट्टी के लिये खाद डालना सही होता है।
पाचन तंत्र और pH:हमारे पाचन तंत्र का pH पाचन में महत्वपूर्ण भूमिका निभाता है। लार का pH हल्का सा क्षारीय होता है जो सैलिवरी एमाइलेज के काम करने के लिये जरूरी होता है। आमाशय में हाइड्रोक्लोरिक एसिड के स्राव के कारण pH अम्लीय होता है। आमाशय के एंजाइम अम्लीय माध्यम में ही काम कर पाते हैं। छोटी आंत का pH क्षारीय होता है जो छोटी आंत के एंजाइम के सही ढ़ंग से काम करने के लिये जरूरी होता है। यदि आमाशय में हाइड्रोक्लोरिक एसिड का अत्यधिक स्राव होता है तो इससे हाइपरएसिडिटी हो जाती है। मिल्क ऑफ मैग्नीशिया या कोई अन्य एंटासिड लेने से हाइपरएसिडिटी के लक्षणों से राहत मिलती है। मिल्क ऑफ मैग्नीशिया तथा अन्य एंटासिड क्षारीय पदार्थ होते हैं। वे आमाशय के अम्ल को उदासीन करके हाइपरएसिडिटी से राहत दिलाते हैं।
pH और दंत क्षय:यदि मुँह के अंदर का pH 5.5 से कम हो जाता है तो इससे दंत क्षय होता है। हमारे मुँह में कई बैक्टीरिया रहते हैं। ये बैक्टीरिया दांतों में फंसे हुए भोजन के टुकड़ों को खाते हैं। ऐसा करते समय ये बैक्टीरिया एसिड निकालते हैं जिससे मुँह का pH कम हो जाता है। अम्लीय माध्यम से दांत के इनामेल को नुकसान पहुँचता है और समय बीतने के साथ दंत क्षय होता है। टूथपेस्ट क्षारीय होने के कारण दंत क्षय की रोकथाम करते हैं।
जंतुओं और पादपों द्वारा आत्मरक्षा: कई जंतु और पादप अपनी रक्षा के लिये अम्ल का इस्तेमाल करते हैं। उदाहरण के लिये; चींटी के डंक में मिथानोइक एसिड होता है जिसके कारण दर्द होता है। इसी तरह, नेटल के पत्तों के ऊपर चुभने वाले रोएँ होते हैं जिनसे मिथानोइक एसिड निकलता है। चींटी के काटने के स्थान पर बेकिंग सोडा मलने से दर्द से आराम मिलता है क्योंकि बेकिंग सोडा क्षारीय होने के कारण अम्ल को उदासीन कर देता है।